Mitokondriedonasjon er ein metode som gjer at kvinner med genfeil i DNA-et i mitokondriane kan få biologiske barn utan sjuke mitokondrium. Metoden overfører cellekjernen frå kvinna si eggcelle til ei donor-eggcelle med friske mitokondrium. Metoden er forbode i Noreg i dag.
Metoden blir kalla mitokondriedonasjon, men i praksis er det snakk om ei cellekjerneoverføring gjort i samband med assistert befrukting. Cellekjernen i eggcella frå kvinna som skal bli mor blir overført til ei kjernelaus eggcelle frå ein donor som har friske mitokondrium. I ei vurdering om bruk av mitokondriedonasjon er både ein diskusjon om tryggleik for barnet som blir til, og ein etisk diskusjon om arveleg genetisk endring av menneske viktige spørsmål.
Kva er mitokondrium?
Mitokondrium er som små kraftverk i cellene våre som omset energi frå maten me et, til energi som cellene kan nytte. Mitokondrium er ein type organell, som ligg utanfor cellekjernen i cella sitt cytoplasma. Celler med høgt energibehov, som til dømes muskel- og nerveceller, har fleire mitokondrium enn celler med lågt energibehov. Nokre menneske har meir effektive mitokondrium enn andre, og kan produsere energi meir effektivt.
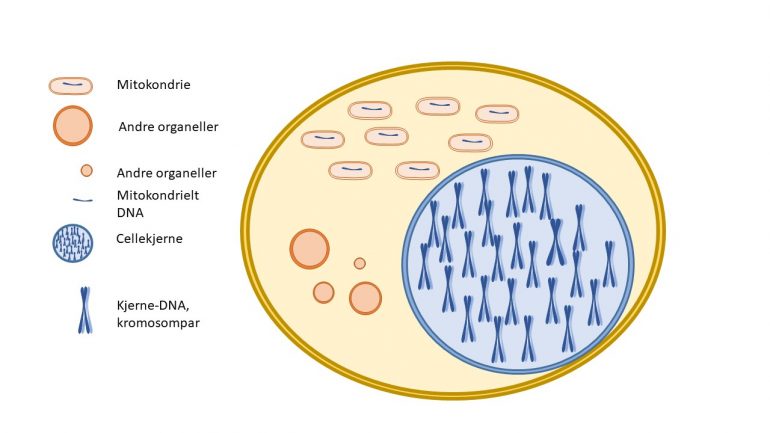
Alle menneske arvar mitokondria sine frå mor. Medan ei eggcelle inneheld om lag 100 000 mitokondrium, har sædcellene berre eit fåtal, naudsynte for å gi cellene rørsleevne til å symje fram til eggcella. Desse er lokalisert i midten av sædcella og følgjer derfor som hovudregel ikkje med når sædcella sitt hovud smeltar saman med eggcella.
Dei fleste proteinkodande gena som er naudsynte for mitokondria sin funksjon (>1000 gen) ligg saman med alle dei andre gena våre i cellekjernen sitt DNA. Men mitokondria har også sitt eige DNA (kalla mitokondrielt DNA) med om lag 16 500 basepar som til saman dannar eit sirkulært DNA-molekyl med 37 gen. Kvart mitokondrium har mellom 2-10 kopiar av dette DNA-molekylet. Til samanlikning har DNA-et i ei cellekjerne om lag tre milliardar basepar, organisert i 23 kromosompar, som til saman har mellom 19 000 – 20 000 gen.
Mitokondriesjukdom
Mitokondriesjukdom skuldast genfeil i DNA-et som inneheld oppskrifta til protein som har ei viktig oppgåve i mitokondria. Desse proteina er viktige for korleis mitokondria fungerer. Genfeila kan oppstå både i DNA-et i cellekjernen og i det mitokondrielle DNA-et, men det er berre for tilfelle der genfeilen har oppstått i det mitokondrielle DNA-et at mitokondriedonasjon kan vera til nytte. Typisk for mitokondriesjukdommar er at dei rammar organ som krev mykje energi, som til dømes musklar, auge, hjarte og nervesystemet. Kor alvorleg sjukdommen er, er avhengig av kor dårleg mitokondria fungerer. Dei mest alvorlege formane for mitokondriesjukdom byrjar tidleg i livet og er som oftast dødeleg. Gravide som er mitokondriesjuke sjølve, har auka risiko for spontanabort og andre svangerskapsrelaterte komplikasjonar. Nokre barn kan vera sjuke frå fødselen av, medan andre kan få gradvise symptom.
Til no kjenner me til om lag 50 ulike mitokondriesjukdommar, inkludert dei som skuldast genfeil i kjerne-DNAet. Då sjukdommane kan ha forskjellige symptom og ulik alvorsgrad, er det truleg at nokre pasientar med mitokondriesjukdom ikkje har fått ein diagnose, eller har fått feil diagnose. I dag er tilbodet til pasientar med mitokondriesjukdom avgrensa til behandling retta mot symptoma sjukdommen gir. Det finst enda ingen årsaksretta behandling, men fleire genterapiar retta mot spesifikke genfeil i ulike sjukdommar er under utprøving.
Mitokondriedonasjon
Ved å nytte mitokondriedonasjon er det mogleg å redusere, og potensielt fjerne, risikoen for at mitokondrium med genfeil i det sirkulære mitokondrielle DNA-et overførast til barnet. Metoden er, trass i namnet, ikkje å donere friske mitokondrium, men å overføre kjerne-DNA frå kvinna som ønskjer barn til eit kjernelaust donoregg med friske mitokondria og mitokondrielt DNA utan genfeilen. Metoden er heller ikkje ei behandling som kan utførast på eit mitokondriesjukt barn, då overføringa skjer før det befrukta egget blir sett inn livmora til kvinna.
Dei finnast fleire teknikkar for å gjere ei slik kjerneoverføring. Felles for dei er at ein nyttar in vitro fertilisering (IVF) til å hente ut modne eggceller frå kvinna som skal bli mor og befruktar eggcella med sæd i laboratoriet. I motsetnad til vanleg IVF treng ein og eit donert egg frå ei kvinne med friske mitokondrium.
Den vanlegaste metoden i bruk i dag blir kalla Pronuclear Transfer – PNT. Ved PNT blir modne eggceller henta ut frå både kvinna som skal ha barn og ein eggdonor som har friske mitokondrium, og eggceller frå begge kvinnene blir befrukta med sæd frå far. Først etter befrukting flyttar ein cellekjernen med mors kjerne-DNA inn i donorcella med friske mitokondria (sjå figur).

Eit barn født etter mitokondriedonasjon vil slik ha arvestoff frå tre ulike personar: kjerne-DNA (som kodar for meir enn 99.9% av proteina i kroppen) frå den biologiske mora og faren, og det sirkulære mitokondrielle DNA-et (som kodar for 13 protein som er viktige for mitokondriefunksjon) frå donoren.
Det er mogleg at nokre sjuke mitokondrium blir med når cellekjernen blir overført. Då vil det befrukta egget kunne innehalde ei blanding av friske mitokondrium frå donor og nokre sjuke mitokondrium frå den blivande mora, noko som kallast heteroplasmi. Ved heteroplasmi vil andelen av sjuke mitokondrium og friske mitokondrium vere avgjerande for om barnet blir sjukt og i tilfelle kor alvorleg.
I 2015 blei Storbritannia det første landet som aktivt tillet mitokondriedonasjon ved lov, og i 2022 følgde Australia etter. Metoden er der eit tilbod til mitokondriesjuke kvinner som har særs høgt sannsyn for å få sjuke barn. I ein del andre land er ikkje mitokondriedonasjon spesifikt vorte tillate, men det har heller ikkje vorte forbode. Det første kjende barnet som vart fødd etter bruk av mitokondriedonasjon har foreldre frå Jordan, egget vart befrukta i New York og sett inn i kvinna si livmor i Mexico.
I 2025 blei ein vitskapleg studie frå Newcastle Fertility Center i Storbritannia publisert, der 22 kvinner hadde gjennomgått mitokondriedonasjon (PNT) og IVF. Åtte av desse blei gravide og på det tidspunktet studien blei publisert, var til saman åtte friske barn fødde (inkludert eit tvillingpar), medan ei av kvinnene framleis var gravid. Studien har vorte omtala som ein milepæl for mitokondriedonasjon, men mange fagpersonar understrekar samstundes at dette framleis er ein eksperimentell teknikk som treng fleire kliniske utprøvingar. Det finst ikkje noko tilgjengeleg register for kor mange barn som er fødde etter mitokondriedonasjon på verdsbasis, men det er også rapportar om barn fødde etter mitokondriedonasjon i Kina, Ukraina og i Hellas.
Etiske vurderingar

Arvelege endringar i genmaterialet
Mitokondriedonasjon førar til arvelege genetiske endringar. Viss barnet som blir fødd er ei jente, inneber det at endringane går i arv til vidare generasjonar. Det strir mot Europarådet sin Biomedisinkonvensjon og UNESCO si verdserklæring om bioetikk og menneskerettar. Argument mot å tillate arvelege genetiske endringar er mellom anna at konsekvensar og skadeverknadar for både enkeltindivid, slekt eller samfunnet er ukjende og vanskeleg å føreseia.
Nokre meiner at dei etiske innvendingane mot arvelege genetiske endringar ikkje gjeld for mitokondriedonasjon, fordi endringane skjer i mitokondria sitt DNA og ikkje i kjerne-DNA-et. Andre meiner at ettersom metoden inneber overføring av cellekjernen til eit egg med anna mitokondrie-DNA, så er det ingen prinsipiell skilnad mellom mitokondriedonasjon og andre arvelege genetiske endringar som det har vore stor einigheit om at ikkje er greitt.
Medisinsk tryggleik
Mitokondriedonasjon er ikkje tillate i Noreg, men i 2020 gjorde Stortinget eit vedtak om at regjeringa skal arbeide for å endre Biomedisinkonvensjonen, eller korleis den skal forståast, slik at mitokondriedonasjon kan bli tillate i Noreg når «metoden er trygg og faglig forsvarlig.»
Generelt blir nye medisinske behandlingar vurdert og godkjent dersom den potensielle nytta av behandlinga for ein sjuk person er høgare enn risikoen. For mitokondriedonasjon er det fleire høve som gjer denne vurderinga komplisert. Metoden er behandling for barnløyse, grunna i faren for at kvinna vil få eit barn med alvorleg sjukdom. Barnet eksisterer ikkje på det tidspunktet mitokondriedonasjon blir utførd og utan behandling vil aldri barnet eksistere. Den direkte nytta av behandlinga tilkjem slik kvinna eller paret.
Risikoen vil derimot først og fremst gjelde for barnet, og for jentebarn også hennar etterkommarar. Korleis skal denne typen nytte og risiko vurderast? Når skal ein kunne fastslå at ei slik behandling er trygg? Etter at barnet er vaksen? Etter at endå ein generasjon har blitt fødd? Sidan det er snakk om arvelege genetiske endringar vil desse, for jenter, også følgje vidare generasjonar. Blir det annleis om ein bestemmer å berre lage gutebarn slik at endringa stoppar med barnet som blir fødd og ikkje går vidare i generasjonane?
Fleire, mellom anna ein EU-rapport om arveleg genredigering publisert i 2021, peiker på at nytte og risiko må inngå i ei vurdering av proporsjonalitet. Metoden må då sjåast i lys av sjukdommane sitt alvor, som for mitokondriesjukdommar varierer mykje, og i fråværet av alternative behandlingsmetodar. I ei slik vurdering vil nokre vekte sistnemnde faktorar høgare, medan andre vekter usikkerheita rundt nytte og risiko høgare – og dermed konkludere ulikt om og når mitokondriedonasjon er trygg og fagleg forsvarleg.
Du kan lese meir om dei etiske vurderingane rundt mitokondriedonasjon i Bioteknologirådet si fråsegn «Mitokondriedonasjon i Norge: biologiske, etiske og juridiske problemstillinger«.
Spørsmål til diskusjon
- Nokon meiner at ei viktig etisk grense blir kryssa dersom ein tillet genetiske endringar i arvematerialet til menneskje. Eksisterer slike grenser, og er dei i så fall relevante?
- Sidan mitokondria berre arvast frå mor, meiner nokre at metoden kan tillatast dersom det berre fødast guteborn. Kva meiner du om ein slik form for kjønnsseleksjon?
- Vurderinga om mitokondriedonasjon er trygg og forsvarleg er kompleks. Kven meiner du bør ha ansvaret for å ta ein slik avgjerd? Er det ei medisinfagleg avgjersle, ei etisk avgjerd eller er den politisk?
Innhaldet på denne sida vart sist oppdatert i desember 2025. Send oss ein e-post dersom du har spørsmål eller kommentarar til innhaldet.