En gendriver er en genvariant som nedarves hyppigere i en populasjon enn de vanlige lovene for arv og genetisk variasjon skulle tilsi. Dette kalles gendrift, og er et naturlig fenomen. Ved å bruke genteknologi kan man lage gendrivere for å spre ønskede genetiske endringer i store populasjoner av ville planter og dyr.
Gendrivere kan brukes til alt fra å utslette sykdomsbærende mygg og skadelige smågnagere, til å bevare utrydningstruede arter som korall og til raskere tilpasning av planter som dyrkes i landbruket. Jo kortere generasjonstid arten har, jo raskere spres endringen. I mange tilfeller er gevinstene åpenbare. Men hva er konsekvensene av å påvirke store økosystemer? Teknologien utfordrer både etablerte metoder for å vurdere risiko og eksisterende regelverk, samt at den reiser svært vanskelige etiske problemstillinger. Hvordan regulerer man bruken av en slik teknologi, når spredningen av en gendriver ikke tar hensyn til landegrenser? Du kan lese mer om gendrivere i GENialt #4-2024 eller lytte til denne episoden av Biotekpodden:
Gendrift og genetisk variasjon
Genetisk variasjon i en vill populasjon styres i hovedsak av to prinsipper: tilfeldige mutasjoner og seksuell formering med etterfølgende naturlig seleksjon. Ulike mekanismer, både ytre faktorer som stråling og miljøgifter og normale prosesser i en celle, kan føre til at det oppstår mutasjoner i arvestoffet. De aller fleste mutasjoner har enten ingen effekt eller negative konsekvenser for organismen, og vil som regel forsvinne ut av populasjonen over tid. Dersom en mutasjon derimot gir en genvariant som gir organismen et konkurransefortrinn, er det sannsynlig at genvarianten kan øke i forekomst fordi avkommene som arver den klarer seg bedre og får flere levedyktige etterkommere enn avkommene uten mutasjonen. Dette kalles naturlig seleksjon.
Hvor raskt en endret genvariant sprer seg i en populasjon, er likevel begrenset av at et individ kun bidrar med halvparten av det genetiske materialet til sitt avkom – såkalt mendelsk arv (figur 1 – normal genetisk arv). At enhver organisme som formerer seg seksuelt får genene sine fra to ulike foreldre, er med på å bidra til genetisk variasjon i en bestand (se temaside om arv og genetikk).
Gendrivere følger ikke de normale arvelovene fordi de øker sannsynligheten for at en genvariant går i arv fra forelder til avkom til over de vanlige 50 prosent. Slik kan mutasjoner spres i en populasjon mye raskere enn under normale betingelser.
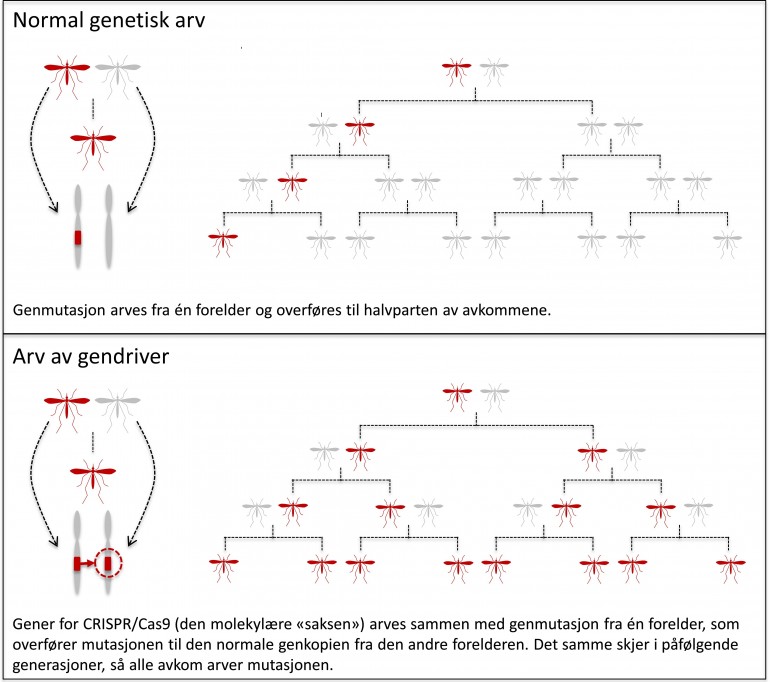
Med genredigeringsverktøyet Crispr har det blitt mulig å lage effektive gendrivere med genteknologi (les mer om Crispr og genredigering her). Når man skal lage en gendriver så setter man både genvarianten med den ønskede egenskapen og hele Crispr-systemet inn i arvestoffet til en organisme. Det fører til at avkommet til denne organismen både vil få den ønskede genvarianten, og at Crispr-systemet vil endre genvarianten avkommet arvet fra den andre forelderen på tilsvarende måte. Dermed vil begge versjonene av genet være av den ønskede varianten, og vil arves av alle avkom i neste generasjon. I praksis innebærer dette at man overstyrer begge prinsippene for genetisk variasjon i en populasjon; mutasjoner kan målrettes, og er derfor ikke tilfeldige, og naturlig seleksjon er ikke lenger en avgjørende faktor for om en egenskap kan øke i frekvens i populasjonen. Gendrivere basert på genredigeringsteknologi gjør det derfor i teorien mulig å modifisere genene i så godt som alle individene i en vill populasjon, med en hastighet styrt av artens generasjonstid.
Crispr-baserte gendrivere kan imidlertid kun brukes i organismer som reproduserer seg seksuelt. Dette utelukker mikroorganismer som bakterier og virus, men omfatter de fleste planter og dyr.
Hvordan lage en Crispr-basert gendriver?
Her bruker vi eksempelet med en Crispr-basert gendriver som skal hindre mygg i å spre malaria. Første oppgave er å lage en bit med DNA. Dette DNA-et skal inneholde både gensaksgenet, et veiledermolekyl som viser hvor det skal kuttes i DNA-et og genet som koder for egenskapen som vi ønsker skal spres i populasjonen, i dette tilfellet en gift mot parasitten som forårsaker malaria.
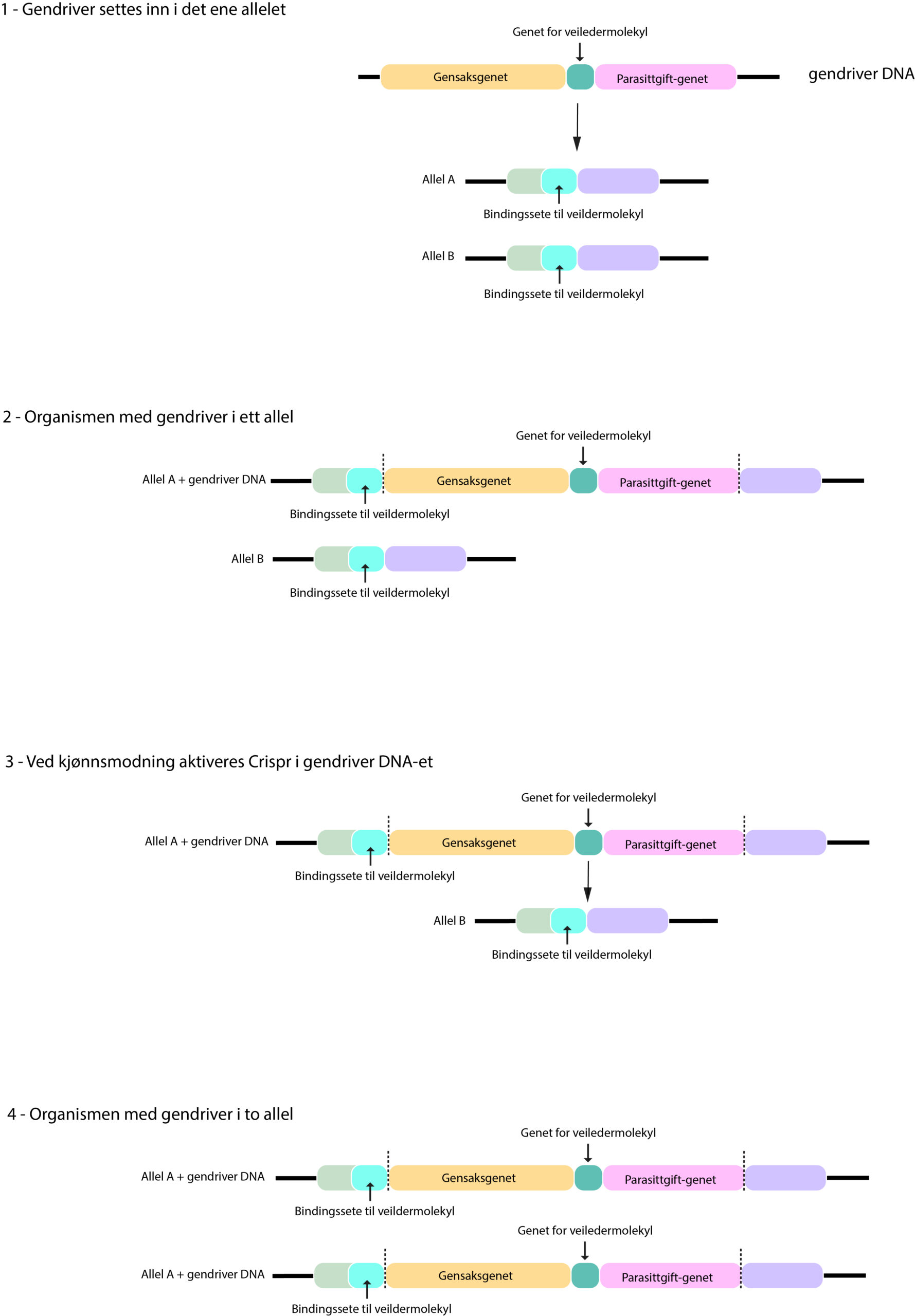
Etter at det nye DNA-et har blitt laget i laboratoriet, så setter man DNA-biten inn på ønsket plass i genomet i et myggegg (1). Myggen som klekkes fra dette egget vil nå ha én genvariant (et allel) med gensaksgenet, veiledermolekylet og genet som koder for parasittgiften og én «vanlig» variant av genet nedarvet fra den andre forelderen (2). Men når myggen går gjennom kjønnsmodning og skal lage kjønnsceller, vil DNA-biten med gendriveren leses av og gensaksen aktiveres (3). Gensaksen klipper så i DNA-et i den genvarianten som myggen arvet fra den andre forelderen, cellens reparasjonsmekanismer setter i gang, og kopierer fra genomet som allerede hadde gendriveren. Slik får man en mygg som har gendriveren i begge variantene (allelene) av dette genet og dermed i alle kjønnscellene (4).
Alt avkom av denne myggen vil ha med seg gendriveren videre, og prosessen vil gjenta seg også i deres avkom slik at alle fremtidige generasjoner vil arve både gensaksen, veiledermolekylet og parasitt-giftgenet.
Eksempler på foreslått bruk av gendrivere
Bekjempelse av sykdommer som spres av mygg

Mygg er bærere av mikroorganismer som kan gi en rekke alvorlige sykdommer, som malaria, dengue-feber, gulfeber og zikafeber. Spesielt malaria er ett av verdens største folkehelseproblemer. I 2015 ble over 200 millioner mennesker smittet, og rundt 500 000 døde, de fleste barn under fem år. Sykdommen forårsakes av parasitter i slekten Plasmodium og det har vist seg svært vanskelig å utvikle effektive vaksiner. Hovedvektoren er myggen Anopheles gambiae, men malaria kan også spres av andre arter i Anopheles-slekten.
Noen forskere ønsker å lage gendrivere som kan hindre spredningen av malaria. Særlig har det vist seg effektivt å bruke teknologien til å lage sterile hunnmygg, som over tid fører til at en art utslettes. Dette har vist seg å fungere svært godt både i laboratoriet, og i forsøk i større skala i lukkede bur.
Andre forskere jobber med å utvikle gendrivere for myggarter tilhørende Aedes-slekten, spesielt Aedes aegypti, som er hovedvektoren for spredning av dengue-feber, gulfeber og zikafeber.
Utrydde introduserte arter – for å bevare andre arter
Omtrent 40 prosent av verdens utryddingstruede arter er hjemmehørende på øyer. En av hovedårsakene til at de er truet, er introduserte arter som gnagere (mus og rotter) som har kommet over med skip. Det gjøres en rekke tiltak for å utrydde gnagerne fra øyene, primært ved bruk av rottegift. Effektiviteten av denne strategien er imidlertid begrenset, siden det ikke er mulig å bruke store mengder gift i tett befolkede områder. I tillegg kan giften også skade andre dyrearter.

Både forskere og interesseorganisasjoner ønsker å utvikle gendrivere i mus og rotter for å utrydde dem fra øyene. Ett eksempel er en gendriver som gjør at det bare fødes hanner, og som derfor vil utslette populasjonen over tid. New Zealand, som har som mål å bli kvitt alle fremmede rovdyr og invasive gnagere innen 2050, vurderer å bruke gendrivere som en del av strategien.
Landbruk
Det finnes flere mulige bruksområder for gendrivere i landbruket. Ett forslag er å bruke dem til å reversere sprøytemiddelresistens i ugress og insekter, eller til å utrydde slike skadegjørere. Et annet er å spre ønskede egenskaper i kulturplanter mye raskere enn man får til med tradisjonelle avlsmetoder.
Nytte mot risiko
Gendrivere kan spre menneskevalgte genetiske egenskaper i naturen raskere enn ved vanlig arv. Det gjør at gendriver-teknologi, kanskje mer enn noen annen teknologi, gjør at vi må vurdere hvordan nytte skal veies mot risiko.
Utviklingen av gendriver-teknologien går raskt, men det er ennå ikke gjort feltstudier av hvordan gendrivere vil kunne påvirke økologi, populasjonsdynamikk og evolusjon. Det er mange komplekse faktorer som vil spille inn, og disse vil variere avhengig av blant annet art, hvilken genetisk egenskap som endres, geografi og interaksjoner i ulike økosystemer. For eksempel vil det kunne antas at en gendriver kan få store konsekvenser dersom den brukes på en nøkkelart i et økosystem. En gendriver kan imidlertid antas å ha mindre konsekvenser om den blir brukt for eksempel for å utrydde en introdusert art som forstyrrer et økosystem. Siden levende organismer ikke lar seg begrense av nasjonale grenser, er det også relevant for en risikovurdering om en gendriver ønskes brukt for å utrydde en uønsket art på en øy (for eksempel rottene på New Zealand) eller på en del av et stort kontinent (som malariamygg i Afrika).
Gendrivere er laget for å spres raskt i store populasjoner, og det arbeides derfor med å utvikle kontrollmekanismer for å kunne begrense spredningen om det skulle bli nødvendig. Ett forslag er at man kan ha klar en ekstra gendriver som kan reversere den første, med andre ord endre genet tilbake til den originale versjonen (som et «genetisk viskelær»). Et annet forslag er system som kalles «daisy-drives», gendrivere som stanser etter et visst antall generasjoner fordi de er designet til å miste deler av DNA-et for hver gang de kopieres. Et tredje alternativ er å bevare originale eksemplarer av arten som endres, slik at de kan settes ut hvis noe skulle gå galt.
Ulike meninger og mye debatt
Noen mener at gendrivere medfører så stor usikkerhet og uforutsigbare konsekvenser at det prinsipielt ikke kan rettferdiggjøres å ta slik teknologi i bruk, uavhengig av mulig nytteverdi for mennesker og også for naturen selv. Andre mener at nyttepotensialet er så betydelig at det rettferdiggjør videre forskning, både i laboratoriet og i feltforsøk. For eksempel har Bill & Melinda Gates Foundation gitt 75 millioner dollar til forskerne som utvikler en gendriver som skal utrydde en naturlig forekommende myggart fordi den sprer malaria i mennesker. Målet til forskerne er at de skal få godkjenning om bruk rundt år 2030 når omfattende forskning og testing har blitt gjennomført, og etter omfattende dialog med myndigheter og lokalbefolkningen i de berørte områdene.
Det er uenighet om eksisterende internasjonale GMO-avtaler er egnet til å regulere gendrivere, og problemstillingene diskuteres derfor i mange internasjonale fora. I 2018 ble et forslag om et midlertidig globalt totalforbud (moratorium) mot å slippe ut organismer med gendrivere nedstemt i FN. De fleste land godkjente imidlertid en avtale som forplikter alle til å gjennomføre en risikovurdering av enhver gendriver som vurderes godkjent nasjonalt.

Spørsmål til diskusjon:
- Synes du vi bør bruke gendrivere for å utrydde en myggart dersom det vil hindre spredning av malaria hos mennesker? I tilfelle hvorfor/hvorfor ikke?
- Er det etisk forskjell på å utrydde en introdusert art som gjør skade på det lokale økosystemet (som rottene på New Zealand) og det å utrydde en ikke-introdusert art som gjør skade (som mygg som kan spre sykdom)?
- Er det etisk forsvarlig å motsette seg all bruk av en teknologi som potensielt kan løse problemer knyttet til folkehelse og bevaring av naturen? I tilfelle hvorfor/hvorfor ikke?
Innholdet på denne siden ble siste oppdatert i september 2025.
Send oss en epost hvis du har spørsmål eller kommentarer til innholdet.




